Histidin
Nu om dage er Histidin et emne, der har fået stor relevans i nutidens samfund. Med tiden har Histidin fået en grundlæggende rolle i forskellige aspekter af dagligdagen, hvad enten det er på arbejdspladsen, i den teknologiske kontekst, i det personlige liv eller på et hvilket som helst andet område. Vigtigheden af Histidin har overskredet barrierer og fordomme og er blevet et emne af almen interesse, der kræver analyse og refleksion. I denne artikel vil vi udforske forskellige perspektiver på Histidin og dets indflydelse på livet i dag.
| Histidin | |
|---|---|
| |
| Generelt | |
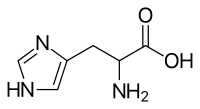
| Systematisk navn | 2-amino-3-(3H-imidazol-4-yl)propansyre |
| Andre navne | Imidazolalanin |
| Molekylformel | C6H9N3O2 |
| Molmasse | 155,16 g/mol |
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |
Histidin (forkortet His og H) er en af de 20 standardaminosyrer i proteiner. I ernæring betragtes histidin som en af de essentielle aminosyrer. Den kodes for med CAU eller CAC.
Histidin blev første gang isoleret af tyskeren Albrecht Kossel i 1896.
Kemiske egenskaber
Imidazolsidekæden og den relativt neutrale pKa på 6,0 betyder at små ændringer i pH omkring fysiologisk pH resulterer i ændringer af histidins ladning, da denne ved svagt sure (og herunder) betingelser protoneres. Dette gør den anvendelig i active sites i enzymer, hvor den uden de store ændringer kan modtage og fraspalte en proton.