Svovlkulstof
I dagens artikel skal vi dykke ned i den fascinerende verden af Svovlkulstof, et emne, der har fanget opmærksomheden hos både eksperter og fans. Siden dets fremkomst har Svovlkulstof vist sin indflydelse på forskellige aspekter af samfundet, videnskaben, kulturen og historien. Gennem årene har det været genstand for debat, undersøgelser og forskning, og dets indflydelse har fortsat udviklet sig over tid. I denne dybdegående udforskning af Svovlkulstof vil vi undersøge dens oprindelse, dens relevans i nutidens verden og de forskellige perspektiver, der eksisterer omkring dette emne. Forbered dig på at fordybe dig i en rejse, der lover at overraske, begejstre og opdrage, når vi sammen opdager det spændende univers i Svovlkulstof.
| Svovlkulstof | |
|---|---|
| Synonymer | carbondisulfid |
| Struktur | 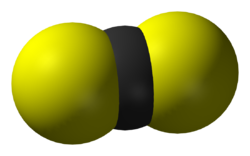
|
| Kemisk formel | CS2 |
| Farve | Farveløs |
| Fysiske egenskaber | |
| Molvægt | 76,13 |
| Smeltepunkt | −111,61 °C |
| Kogepunkt | 46,24 °C |
| Massefylde | 1266 |
| Damptryk | 48,1 kPa (25 °C) |
| Flammepunkt | -43 °C |
| Antændelsestemperatur | 102 °C |
| Diverse | |
| CAS-nummer | 75-15-0 |
| Tilstand ved stuetemp. | væske |
Svovlkulstof eller carbondisulfid (kemisk formel: CS2) er en giftig og brandfarlig væske, der bruges som opløsningsmiddel.
Fremstilling
Fremstilling af svovlkulstof sker via direkte reaktion mellem svovl og kul ved en temperatur på 1200 oC:
- 4C + S8 → 4CS2
En anden metode, som kræver en lavere temperatur, er at lade metangas boble gennem flydende svovl blandet med silicagel eller aluminiumoxid som katalysator:
- 2CH4 + S8 → 2CS2 + 4H2S
Herved dannes også giftig hydrogensulfidgas som et biprodukt.
| Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |
| Infoboks uden skabelon Denne artikel har en infoboks dannet af en tabel eller tilsvarende. |